La Retinite Pigmentosa è tra le degenerazioni visive più frequenti ed è ancora tra le cause principali di cecità nel mondo e solo in Italia affligge circa 30mila persone.
La Diffusione della malattia, secondo le statistiche internazionali, colpisce circa una persona su 4.000 sane e nel nostro paese, dove non mancano i matrimoni tra i consanguinei, l’incidenza di questa patologia ereditaria risulta ancora più elevata, al punto da farla annoverare, dal 1985, tra le malattie sociali della penisola. Molto spesso essa compare tra la pubertà e l’età matura, ma non sono assolutamente rari gli esempi di bambini colpiti nella prima infanzia.

La Retinite Pigmentosa è una malattia genetica che colpisce la Retina, la parte posteriore dell’occhio, sensibile alla luce e deputata a convogliare i segnali luminosi verso il nervo ottico e poi al cervello dopo averli trasformati in stimoli elettrici.
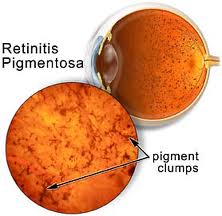
Il termine “Retinite” indica una disfunzione della retina, mentre “Pigmentosa” si riferisce alla caratteristica comparsa, negli stadi avanzati della malattia, di zone abnormi di pigmento nella retina. La degenerazione, riguarda entrambi gli occhi e colpisce i fotorecettori (coni e bastoncelli) e l’epitelio pigmentato retinico uccidendo queste cellule in modo lento e progressivo. La retina subisce così un progressivo deterioramento, perdendo la capacità di trasmettere al cervello le informazioni visive.
I Fotorecettori sono delle cellule sensibili alla luce: i Coni, così chiamati per la loro particolare forma, recepiscono i particolari dell’immagine ed i colori e sono localizzati in maggior densità nella parte centrale della retina, la macula, mentre i Bastoncelli, allungati e affusolati, reagiscono al contrasto tra il chiaro e lo scuro ed al movimento degli oggetti e sono più numerosi nella zona periferica. Grazie a questi ultimi recettori, quelli più colpiti all’inizio della malattia, riusciamo ad avvertire un pericolo che si avvicina con la coda dell’occhio, anche se non siamo in grado di percepirne i particolari.
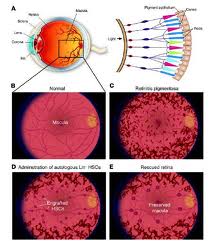
Il sistema fotorecettoriale più colpito è quello dei bastoncelli, coinvolti nella visione notturna. Nelle fasi più avanzate della patologia sono interessati anche i coni, anche se con un meccanismo al momento sconosciuto. I fotorecettori ammalati vanno incontro ad apoptosi: il ritmo della perdita di fotorecettori si può notare dall’assottigliarsi del ONL (Outer Nuclear Layer), lo strato retinico che contiene i fotorecettori, e dall’accumulo di pigmento (rodopsina) sulla retina. Ai coni è demandata la visione diurna e in dettaglio. Si può supporre in via generale che la semplice presenza dei bastoncelli fornisca i segnali di sopravvivenza necessari a mantenere “in vita” i coni. Il primo gene collegato al fenotipo RP venne scoperto ventisei anni fa sul cromosoma X.
Da allora più di 40 geni sono stati messi in relazione con la patologia. Le mutazioni da cui la retinite viene causata possono essere autosomiche recessive, dominanti o legate al cromosoma X. Nella maggior parte dei casi (50-60%) le mutazioni sono autosomiche recessive, seguite in probabilità da quelle dominanti (30-40%) e legate al cromosoma X (5-20%).
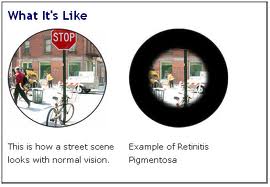
Il Primo Sintomo consiste nella diminuzione della capacità visiva notturna (difficoltà a guidare di sera o a muoversi in locali scarsamente illuminati) fino ad arrivare ad un restringimento del campo visivo periferico (difficoltà a percepire oggetti posti lateralmente o a vedere i gradini scendendo le scale) e, nella fase finale della malattia, in alcuni casi, alla perdita della visione centrale ed alla cecità. Si può accompagnare anche a cataratta o sordità, manifestazioni queste legate direttamente alla retinite pigmentosa. La velocità di progressione della malattia e l’età di comparsa dei sintomi variano in relazione a molti fattori tra cui il modello di trasmissione genetico.
La Diagnosi viene fatta dall’oculista con:
L’esame del Visus, che consiste nella lettura di caratteri di varia grandezza ad una distanza nota. Questo permette di valutare l’acutezza visiva nella porzione centrale della retina;
L’esame del Fondo dell’Occhio, che ha lo scopo di ricercare la presenza delle caratteristiche macchie di pigmento sulla superficie retinica, anche se in talune forme di retinite, queste macchie non sono presenti;
L’esame del Campo Visivo, che permette di valutare la sensibilità retinica ad uno stimolo luminoso sia nella zona centrale che periferica; L’Elettroretinogramma, che consiste nella registrazione dell’attività elettrica della retina in risposta a particolari stimoli luminosi, permettendo di valutare in modo distinto la funzionalità dei due diversi tipi di fotorecettori (i coni ed i bastoncelli). L’elettroretinogramma è un esame molto importante per diagnosticare la Retinite Pigmentosa, poichè anche quando la malattia è ancora nella fase iniziale, il tracciato che ne deriva è quasi sempre estinto e molto appiattito.
La Fluorangiografia, che si effettua tramite l’iniezione per via endovenosa di una sostanza fluorescente con una contemporanea fotografia della retina in tempi diversi. Infatti tramite la circolazione sanguigna, la sostanza fluorescente giunge sino alla retina, rendendo visibili, colorandole, le arterie, i capillari e le vene, nonchè lo stato funzionale delle loro pareti. Si consiglia, inoltre, di ricorrere ad approfonditi Esami Genetici per poter quantificare i rischi di trasmissione della malattia.
Per questa malattia, al momento, siamo solo in grado di contrastare le complicanze ma non di bloccarne gli effetti, ma la ricerca scientifica internazionale sulle terapie geniche, sui trapianti di retina e sulla retina artificiale, consente fondate speranze per il prossimo futuro.
Vi sono diversi filoni di ricerca che lasciano ben sperare:
La Genetica, che si propone di identificare il gene od i geni responsabili della malattia, per poter eventualmente intervenire in seguito con le moderne tecniche dell’ingegneria; I Trapianti, con l’intento di mettere a punto una tecnica che renda possibile il trapianto di tessuto retinico, o per lo meno l’innesto di cellule sane su retine malate; L’Immunologia, che si prefigge di verificare alcune teorie che ipotizzerebbero un’alterazione del sistema immunologico alla base della malattia; La Tecnologia, che potrebbe permetterci, in un prossimo futuro, di impiantare ausili ottici nel nostro occhio.
RHO, il gene per la Rodopsina, è uno tra i geni più associati alla retinite pigmentosa. Mutazioni nel gene RHO provocano generalmente un fenotipo autosomico dominante, con effetto dominante negativo sul funzionamento del fotorecettore. E’ possibile per esempio che l’accumularsi di proteine con folding errato nel reticolo endoplasmatico porti all’attivazione dei pathway apoptotici (Hartong et al., 2006). E’ infatti generalmente riconosciuto che la causa principale della perdita di capacità visive dovuto a retinite pigmentosa sta nel processo dell’apoptosi. I geni del ciclo della visione, se mutati nei bastoncelli, provocherebbero la perdita di visione notturna fin dalla nascita, e la susseguente morte dei fotorecettori a causa dello squilibrio nella fisiologia delle cellule fotorecettoriali causato dalle proteine mal funzionanti. Per questo motivo l’idea dei ricercatori del Tigem è stata quella di costruire un interruttore universale per il gene della rodopsina, capace di spegnere sia quello sano sia quello alterato, indipendentemente dal tipo di errore genetico. E’ stata così sviluppata una tecnologia basata su “proteine artificiali” che legano il DNA in modo da rendere inattivo nelle cavie animali il gene alterato della Rodopsina. Il passo successivo sarà fornire, insieme all’interruttore per lo spegnimento, la versione sana del gene.

Un gruppo di ricercatori dell’Università dell’Oklahoma ha sperimentato un nuovo metodo terapeutico che interviene sul codice genetico ed è in grado di arrestare la degenerazione retinica prima che il soggetto perda la vista. Sono state iniettate delle capsule, in occhi di cavie animali, che hanno raggiunto i fotorecettori retinici riparandoli e prevenendo totalmente la degenerazione dei coni con la tecnica del DNA ricombinante. Questi geni selezionati, infatti, sono capaci di conferire nuove caratteristiche alle cellule riceventi malate, dette appunto ricombinanti, in modo da alterare la sequenza del gene originale e da produrne uno più normale. “Le terapie – spiega il capo delle ricerche Muna Naash – sono state iniettate direttamente nell’occhio delle cavie e trasportate velocemente, in soli 15 minuti, grazie a delle capsule curative che raggiungono e riparano direttamente i fotorecettori della retina, ossia le cellule sensibili alla luce”. La terapia, al momento, è stata sperimentata soltanto sugli animali ma i ricercatori americani non escludono che questa nuova tecnica possa dare dei risultati validi e senza complicazioni anche nella sperimentazione umana.
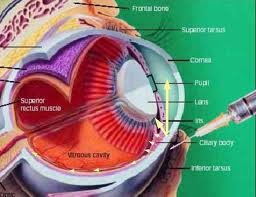
A Londra per la prima volta, in un esperimento condotto su topi, un gruppo di ricercatori è riuscito a ripristinare parzialmente la facoltà visiva, trapiantando negli animali cellule precursori della retina.
Gli scienziati non hanno utilizzato cellule staminali, che in precedenza non avevano dato risultati per questo tipo di problema, ma cellule già parzialmente mature, e quindi, già con una destinazione precisa: i fotorecettori.
E’ da tempo che si tenta il trapianto di cellule nella retina per ricostituire coni e bastoncelli, ma finora non c’erano sono stati progressi significativi. Una delle coordinatrici dello studio, la dottoressa Jane Sowden, si è detta sorpresa dei risultati ottenuti: “Abbiamo riscontrato che la retina matura, che finora si credeva non avesse la capacità di rigenerarsi, è invece in grado di sopportare lo sviluppo di nuovi fotorecettori funzionali”, ha spiegato.
I ricercatori guidati da Robin Ali, dell’istituto londinese, hanno invece pensato di trapiantare cellule “semi-adulte”, cioè già abbastanza sviluppate e avviate a diventare cellule della retina, ma senza aver ancora raggiunto lo stadio di maturazione completa. Ha funzionato: trapiantando cellule della retina, gli scienziati hanno ottenuto un miglioramento parziale della funzione visiva nei topi. Le cellule trapiantate hanno ultimato il loro sviluppo trasformandosi in fotorecettori, e si sono integrate nella retina, allacciando contatti con le terminazioni del nervo ottico, diventando così funzionali.
”E’ una ricerca sorprendente, che in futuro potrebbe portare ad un trapianto per curare la cecità nell’uomo”, ha commentato alla Bbc il professor AndrewBrick dell’università di Bristol. Il cammino verso un’applicazione clinica è ancora molto lungo, ma già nel giro di cinque anni si potrebbero avere i primi sviluppi verso un utilizzo di questa nuova procedura anche sull’uomo.
Un’altra ricerca è quella condotta da un’équipe internazionale di scienziati statunitensi e dell’Arabia Saudita. Attraverso la terapia genica i ricercatori, guidati da Kang Zhang, professore di oftalmologia all’Università della California a San Diego e da Fowzan Alkuraya, a capo dell’unità di genetica dello sviluppo al King Faisal Specialist Hospital and Research Center, sono riusciti a ripristinare le capacità visive in animali affetti da retinite pigmentosa.
Questi ricercatori affermano che la base genetica di questa malattia è una mutazione nella proteina MERTK, che controlla l’eliminazione dei residui di cellule e patogeni. Negli individui affetti da retinite pigmentosa si ha, di conseguenza, l’accumulo di materiale di scarto tra l’epitelio della retina, i coni e i bastoncelli.
La nuova terapia proposta dai ricercatori prevede l’inserimento della versione corretta di MERTK attraverso l’impiego di un virus, in modo da ristabilire la funzionalità di queste cellule. Questo approccio si è già dimostrato efficace in soggetti colpiti da un tipo simile di malattia, l’amaurosi congenita di Leber; dopo averlo sperimentato con successo nei roditori, gli autori dello studio stanno effettuando prove in altri modelli animali. L’obiettivo è di passare il più presto possibile all’applicazione sull’essere umano.
Scienziati e medici del Moorfields Eye Hospital hanno impiantato l’occhio artificiale all’interno dell’occhio naturale, il quale è stato connesso a una microtelecamera posta su un paio di occhiali. Una serie di microscopici elettrodi stimolano i nervi danneggiati della retina, consentendo al segnale di passare lungo il nervo ottico e raggiungere il cervello. Qui come di consueto il segnale viene decodificato e trasformato in immagine. Ciò che una persona vede è tanto più chiaro quanto meno danneggiato è il sistema della retina. Al momento i pazienti sono in grado di distinguere solo ombre del mondo che li circonda, ma ciò significa che il sistema funziona e che potrà essere migliorato entro breve tempo. La speranza è che le persone affette da retinite pigmentosa possano almeno vedere le persone che le circondano e il mondo della propria stanza. Per ora gli scienziati comunque mostrano cautela. Solo fra qualche tempo si capirà sei i due pazienti che si sono sottoposti alla sperimentazione torneranno a vedere nitidamente. Dal punto di vista tecnologico, c’è ottimismo sulla possibilità di ridurre ulteriormente le dimensioni della telecamera e aumentare il numero di elettrodi del dispositivo. Sedici quelli impiantati finora, ma i ricercatori contano di arrivare fino a 60 con la prospettiva di mille, per immagini sempre più pulite.
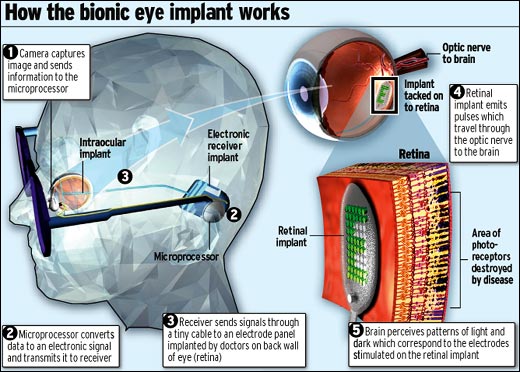
Dal punto di vista farmacologico sono stati proposti vari protocolli terapeutici aventi un effetto sul metabolismo del fotorecettore (Vit.A, antocianosidi, ecc.), ma nessuno si è dimostrato in grado di guarire o di modificare la progressione della malattia.
Secondo alcune ricerche, la terapia con ossigeno (OTI), potrebbe essere di notevole importanza per i dati sperimentali che confermano come l’ossigeno influisce positivamente riducendo il tasso di morte cellulare dei fotorecettori. Per la prima volta usata in terapia da Henshaw nel 1662 con finalità mediche, l’ossigenoterapia iperbarica (OTI) fu molto più tardi impiegata da Junot (1834) come “bagni in aria compressa” in molte città europee quale panacea a molte infezioni.
L’OTI è basata sulla somministrazione di ossigeno puro in ambienti ermeticamente chiusi (camere iperbariche) entro cui, con aria immessa dall’esterno, si aumenta la pressione ambientale.
Tale metodica rende possibile la diffusione dell’ossigeno nei liquidi corporei in concentrazione fino a 15 volte superiore a quella normale. L’ossigeno può così diffondersi anche dove arrivano con difficoltà i globuli rossi, normalmente essenziali per veicolare questo gas vitale.
Tutti questi studi effettuati sia con cellule isolate che con animali da esperimento, hanno evidenziato l’efficacia dell’ossigeno nel salvataggio dei fotorecettori e di converso la tossicità per i fotorecettori di ambienti poveri d’ossigeno anche per retine normali.
La terapia iperbarica, comunque, non ha una efficacia dimostrata nell’uomo, ma è innocua e vi sono individui che ne traggono un lieve beneficio soggettivo.
